(1) 無作為化比較試験等の公表論文
| 1. |
|
Velasquez WS, Cabanillas F, Salvador P, McLaughlin P, Fridrik M, Tucker S, Jagannath S, Hagemeister FB, Redman JR, Swan F, et al. Effective salvage therapy for lymphoma with cisplatin in combination with high-dose Ara-C and dexamethasone (DHAP). Blood. 1988 Jan;71(1):117-22. |
| 2. |
|
Philip T, Guglielmi C, Hagenbeek A, Somers R, Van der Lelie H, Bron D, Sonneveld P, Gisselbrecht C, Cahn JY, Harousseau JL, et al. Autologous bone marrow transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive non-Hodgkin's lymphoma. N Engl J Med. 1995 Dec 7;333(23):1540-5. |
| 3. |
|
Velasquez WS, McLaughlin P, Tucker S, Hagemeister FB, Swan F, Rodriguez MA, Romaguera J, Rubenstein E, Cabanillas F. ESHAP--an effective chemotherapy regimen in refractory and relapsing lymphoma: a 4-year follow-up study. J Clin Oncol. 1994 Jun;12(6):1169-76. : |
| 4. |
|
Aparicio J, Segura A, Garcera S, Oltra A, Santaballa A, Yuste A, Pastor M. ESHAP is an active regimen for relapsing Hodgkin's disease. Ann Oncol. 1999 May;10(5):593-5. |
|
(2) 教科書
| 1. |
|
Armitage JO, Mauch PM, Harris NL and Bierman P: Non-Hodgkin ' s Lymphomas, in DeVita VT Jr, Hellman S, & Rosenberg SA (ed) : Cancer: Principles and Practice of Oncology, Philadelphia, PA, Lippincott Williams & Wilkins, 2001, pp 2256-2315 |
| 2. |
|
Diehl V, Mauch PM, and Harris NL Hodgkin’s disease, in DeVita VT Jr, Hellman S, & Rosenberg SA (ed) : Cancer: Principles and Practice of Oncology. Philadelphia, PA, Lippincott Williams & Wilkins, 2001, pp 2329-2388 |
| 3. |
|
Wooldridge JE: Appendix A: Chemotherapy Programs, in Perry MS (ed) : The Chemotherapy Sourcebook, Philadelphia, PA, Lippincott Williams & Wilkins
この教科書中に掲載されている療法は以下のとおり。
| ・ |
DHAP療法について
|
Dexamethasone , 40 mg/day i.v. days 1-4
Cisplatin , 100 mg/ m2 c.i. i.v. over 24 hours day 1
Cytarabine , 2000 mg/ m2 i.v. q12h x 2, day 2
*Repeat every 21 days. |
|
(参照論文)
|
Cabanillas F, Velasquez WS, McLaughlin P, et al. Results of recent salvage chemotherapy regimens for lymphoma and Hodgkin's disease. Semin Hematol Suppl 1988;25[2 2]:47-50. (http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=retrieve&db=pubmed&list_uids=3041599&dopt=abstract',700,500) |
| ・ |
ESHAP療法について
|
Etoposide , 40 mg/m2 per day i.v. days 1-4
Methylprednisolone (Solumedrol), 250-500 mg/day i.v. days 1-5
Cytarabine , 2,000 mg/ m2 i.v. day 5 (after cisplatin)
Cisplatin , 25 mg/ m2 /day c.i. i.v. days 1-4
*Repeat every 21-28 days. |
|
(参照論文)
|
Velasquez WS, McLaughlin P, Tucker S, et al. ESHAP; an effective chemotherapy regimen in refractory and relapsing lymphoma: a 4-year follow-up study. J Clin Oncol 1994;12(6):1169-1176.
(http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=retrieve&db=pubmed&list_uids=8201379&dopt=abstract',700,500); |
|
|
(3) peer-review journalに掲載された総説、メタ・アナリシス
| 1. |
|
Cabanillas F, Velasquez WS, McLaughlin P, Jagannath S, Hagemeister FB, Redman JR, Swan F, Rodriguez MA. Results of recent salvage chemotherapy regimens for lymphoma and Hodgkin's disease. Semin Hematol. 1988 Apr;25(2 Suppl 2):47-50. |
| 2. |
|
Hagemeister FB.Treatment of relapsed aggressive lymphomas: regimens with and without high-dose therapy and stem cell rescue. Cancer Chemother Pharmacol. 2002 May;49 Suppl 1:S13-20. Epub 2002 Apr 12. Review. |
| 3. |
|
Gisselbrecht C, et al. Improving Second-Line Therapy in Aggressive Non-Hodgkin’s Lymphoma. Semin Oncol 31 (suppl 2):12-16. 2004 |
| 4. |
|
Crawford J. Once-per-cycle pegfilgrastim (Neulasta) for the management of chemotherapy-induced neutropenia. Semin Oncol. 2003 Aug;30(4 Suppl 13):24-30. Review. |
|
(4) 学会又は組織・機構の診療ガイドライン
CDDPもしくはDHAP, ESHAPとしてのガイドラインはないが、救援化学療法に奏効するaggressive non-Hodgkin's lymphoma (NHL)に対する自家造血幹細胞移植併用の大量化学療法とconventional化学療法を比較し、救援化学療法に奏効した症例には大量化学療法をすることが標準的治療であることを検証したParma study (Philip T, et al. N Engl J Med)で使用された救援化学療法がDHAPである。DHAPそのものが他の救援化学療法に比べ最も優れているという報告は無いが、最も代表的な救援化学療法として、他の救援化学療法の第II相試験での論文報告には必ず比較引用がされる。Parma studyの結果を受けて、救援化学療法に奏効するaggressive NHLに対しては自家造血幹細胞移植併用の大量化学療法の実施が標準的治療法となることが、Parma studyのDHAP療法に引き続く大量化学療法を引用する形で日本造血細胞移植学会のガイドライン(造血幹細胞移植の適応ガイドライン、p53)に記載されている。http://www.jshct.com/about_guideline.html |
(5) 総評
再発、難治性の悪性リンパ腫に対するCDDPを含むDHAP療法、ESHAP療法について、今までに報告された試験結果を考察し、以下の理由により有効性、安全性は医学・薬学上、認められると考えられる。
| 1. |
|
90症例の再発性リンパ腫(低悪性度13例、中悪性度72例、高悪性度5例;治療抵抗性52例、寛解後再発38例、20-78歳)に対し、DHAP療法を3-4週間隔で6-10コース実施した結果、%CR, %PRは各31%、26.5%であり、2年生存率は25%であった。主な毒性は骨髄抑制であった。CDDPによる非可逆的なクレアチニン上昇が4例に認められた。治療関連死亡として、好中球減少症に伴う敗血症10例、tumor lysis syndromeに伴う多臓器不全3例、呼吸不全2例が認められた。(注;本試験はG-CSFが上市される以前に実施されており、G-CSFなどの感染予防対策が進歩した現在では、致命的な好中球減少性発熱、重症感染症も発生頻度は低いものと推定される。)Blood. 1988 Jan;71(1):117-22 |
| 2. |
|
122症例の再発難治性リンパ腫(低悪性度34例、低悪志度から中悪性度への組織転化18例、中悪性度67例、高悪性度3例)に対してESHAP療法を実施(奏効症例に対しては3-4週間間隔で最大6-8コースを投与)した結果、%CR, %PRは各37%、27%であり、20ヶ月の観察期間中央値で3年生存率は31%であった。主な毒性は骨髄抑制であった。本試験でもG-CSFは上市されていなかったため使用されず、122例中、治療関連死亡は6例(感染症5例、循環器障害1例)であった。(注;G-CSF使用可能な現在では、速やかな好中球回復が期待可能なため、好中球減少時の感染症死はきわめて低いものと推定される。) J Clin Oncol. 1994 Jun;12(6):1169-76 |
| 3. |
|
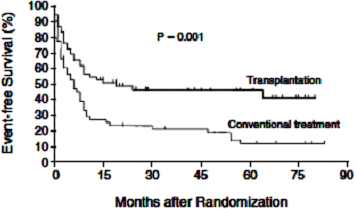
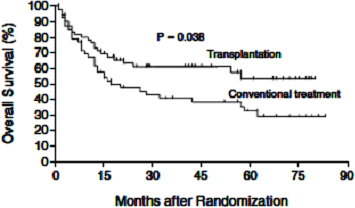
aggressive NHLに対する初回化学療法に治療抵抗性もしくは寛解後再発症例に対して開発されたシスプラチンを含んだ救援化学療法であるDHAP療法、ESHAP療法は評価すべき奏効性を示すが、上記のように2年生存割合もしくは3年生存割合は25-31%と低く、DHAPに奏効した症例に対しては、自家造血幹細胞移植を併用した大量化学療法を実施することが、長期生存を期待できる治療法であることがランダム化比較試験(Parma Study)で検証されている。このランダム化比較試験に先だって、DHAP療法に引き続いて自家骨髄移植併用の大量化学療法を行うpilot studyがParma groupによって再発リンパ腫に対して実施された(Blood. 1991 Apr 1;77(7):1587-92.)。16歳から60歳までの50例に実施された本pilot studyでは、DHAP療法の毒性は許容でき、評価すべき有効性が得られたためランダム化比較試験が実施された。このランダム化比較試験ではaggressive NHLの再発215症例にDHAP療法を2コース実施しCRもしくは部分寛解(PR)となったいわゆるchemotherapy-sensitive再発症例の109例に対し、conventional therapyであるDHAP療法を4コース続けて再発時5 cmを越えるbulky massに照射を加える(involved field radiation therapy, IFRT)群と、IFRT後に自家骨髄移植(ABMT)を併用した大量化学療法(BEAC療法)を実施する群との比較検証が行われた。1995年に報告されたその結果では、5年のevent free survival(eventの定義は再発、増悪、原因を問わない全ての死亡)はABMT群が46%、DHAP群が12%(p=0.001)、overall survivalではABMT群が53%、DHAP群が32%(p=0.038)と2群間に統計学的有意差を認めた。DHAPによる毒性のために、大量化学療法が実施できなかった症例は無く、G-CSFが使用可能であった本試験ではDHAP療法での好中球減少症時の感染症死は認められなかった。N Engl J Med 1995 333:1540-1545 |
| 4. |
|
したがって、これ以後、再発aggressive NHLの救援化学療法反応群には自家造血幹細胞移植併用の大量化学療法を実施することが標準的治療法として確立した。救援化学療法同士の比較試験は実施されていないために、best regimenは確立していないが、Parma studyで使用されたことにより、DHAP療法は再発難治性リンパ腫に対する代表的救援化学療法の一つである。 |
| 5. |
|
CDDPを含む多剤併用化学療法は若年者、成人の広い年齢層の再発難治悪性リンパ腫患者に対して有効な化学療法として、国内外で汎用され、毒性に対する集積は十分であり、腫瘍に対する化学療法に熟知した医師であれば、本剤と多剤併用療法で発生する骨髄抑制、および、悪心・嘔吐、腎毒性を予防、コントロールすることに熟練しており安全性は担保できると考えられる。しかるに、再発難治性悪性リンパ腫に対する本剤の有用性、安全性は医学・薬学上公知であると判断できる。 |
|
| 臨床試験の試験成績に関する資料 |
1
Velasquez WS, Cabanillas F, Salvador P, McLaughlin P, Fridrik M, Tucker S, Jagannath S, Hagemeister FB, Redman JR, Swan F, et al. Effective salvage therapy for lymphoma with cisplatin in combination with high-dose Ara-C and dexamethasone (DHAP). Blood. 1988 Jan;71(1):117-22.
90症例の再発性リンパ腫(低悪性度13例、中悪性度72例、高悪性度5例;治療抵抗性52例、寛解後再発38例、20-78歳)に対し、DHAP療法(デキサメサゾン40 mg/day IV days 1-4、シスプラチン100 mg/m2 持続点滴 1日 day 1、シタラビン 2000 mg/m2 IV 1日2回12時間毎、1日間 day 2)を3-4週間隔で6-10コース実施した結果、%CR, %PRは各31%、26.5%であり、11ヶ月の観察期間中央値での2年生存割合は25%であった。低腫瘍量かつ正常LDH値の症例では%CRは67%、2年生存割合が61%と優れた成績を示したが、高腫瘍量かつ高LDH値の症例では%CRは0%、1年生存割合も5%と予後不良の成績を示した。主な毒性は骨髄抑制で、300/μl未満の好中球減少症、20,000/μl未満の血小板減少症は各々、53%、39%であった。好中球減少症に伴う細菌感染もしくは真菌感染症は28例に認められ、10例が敗血症で死亡した。なお、本試験当時、G-CSFは上市されていなかったため、G-CSFなどの好中球増加成長因子は使用されなかった。CDDPによる治療前値の2倍以上のクレアチニン上昇が14例に認められ、非可逆的なクレアチニン上昇が4例(4.4%)に認められたが、60歳を超える高齢症例や、CDDPの蓄積投与量が300mg/m2を越える症例に多く認められた。CDDP の毒性として軽度の脱力は高頻度で認められたが、CDDPによると思われる重症の末梢神経炎が4例に認められ、これらの症例ではCDDPは中止された。耳鳴りが4例では強く認められ、別の3例では重度の難聴が認められた。高腫瘍量かつ高LDH値の症例の5例でtumor lysis syndromeが認められ、内3例が死亡した。治療関連死亡として、好中球減少症に伴う敗血症10例、tumor lysis syndromeに伴う多臓器不全3例、呼吸不全2例が認められた。シタラビンによる急性神経毒性は稀であり、1例に重症の小脳失調を認めたが、その症例は以前にリンパ腫の髄膜浸潤のためにシタラビンの髄腔内投与を受けたことがある症例であった。(Blood. 1988 Jan;71(1):117-22)。本試験が実施された1984年から86年においては、G-CSFが未開発であり、G-CSFをはじめとする感染予防の薬品・技術が進歩した現在では好中球減少時の感染症死亡率はきわめて低いものと推定される。また、本試験は78歳までの症例に対して実施され、高齢者を中心に非可逆性の腎毒性を認めたが、自家造血幹細胞移植の適応年齢である60-65歳未満の症例で、かつDHAP2コースで奏効を示す症例には大量化学療法を実施することになるため、CDDPの蓄積投与量は200 mg/m2であり、重篤な非可逆的腎毒性の頻度は減少するものと推定される。
2.
Philip T, Guglielmi C. Hagenbeek A. et al. Autologous bone marrow transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive non-Hodgkin’s lymphoma. N Engl J Med 1995 333:1540-1545
Parma グループはaggressive NHLの再発215症例にDHAP療法(dexamethasone、high-dose Ara-C、CDDP)を2コース実施しCRもしくは部分寛解(PR)となったいわゆるchemotherapy-sensitive再発症例の109例(全奏効割合58%)に対し、conventional therapyであるDHAP療法を4コース続けた後に、再発時5 cmを越えるbulky massに照射を加える(involved field radiation therapy, IFRT)群と、IFRT後にABMTを併用した大量化学療法(BEAC療法)を実施する群とのランダム化比較試験を実施した。1995年に報告されたその結果では、5年のevent free survival(eventは再発、増悪、原因を問わない全ての死亡)はABMT群が46%、DHAP群が12%(p=0.001)、overall survivalではABMT群が53%、DHAP群が32%(p=0.038)と2群間に統計学的有意差を認めた。
これ以後、再発aggressive NHLの救援化学療法反応(奏効)群には自家造血幹細胞移植併用の大量化学療法を実施することが標準的治療法として確立した。異なった救援化学療法をランダム化比較した研究報告はないため、bestの救援化学療法は確立していないが、この研究で採用された救援化学療法であるDHAP療法がこれ以後、救援化学療法の代表的治療レジメンの一つとされている。Parma studyで2コースのDHAP療法後に大量化学療法を受けた55例中5例にgrade 2以下の腎毒性が認められたが、計6コースのDHAP療法を受けた54例ではgrade 3の1例を含む14例に腎毒性を認めた。55症例中で、大量化学療法が実施できなかった症例は6例であったが、原疾患の再発、増悪、幹細胞採取不良などが原因であり、DHAPによる毒性のために、大量化学療法が実施できなかった症例は無かった。
3.
Velasquez WS, McLaughlin P, Tucker S, Hagemeister FB, Swan F, Rodriguez MA, Romaguera J, Rubenstein E, Cabanillas F. ESHAP--an effective chemotherapy regimen in refractory and relapsing lymphoma: a 4-year follow-up study. J Clin Oncol. 1994 Jun;12(6):1169-76.
CDDPを使用したDHAP療法以外の多剤併用救援化学療法としてESHAP療法がある。本レジメンはDHAP療法を開発したM. D. Anderson Cancer Centerにより開発されたもので、DHAP療法で認められた腎毒性などの有害事象の軽減を目的としてCDDPを4日間の持続点滴とし、Ara-CもDHAPの1日2回投与を、1日1回投与に減量して骨髄毒性の軽減を図り、抗腫瘍効果の増強を目的としてetoposideを併用した治療法である(etoposide 40mg/m2点滴IV, 4日間 (days 1-4), methylprednisolone 250-500 mg/ day点滴IV, 5日間 (days 1-5), cisplatin 25 mg/m2持続点滴, 4日間(総量100 mg/m2 (days 1-4), cytarabine 2 g/m2 持1日1回、1日間 (day5)。122症例の再発難治性リンパ腫{低悪性度34例、中悪性度67例、高悪性度3例、低悪性度からの組織転化18例;寛解後再発69例、治療抵抗性53例;年齢18-78歳(中央値53歳)}に対してESHAP療法が投与された。奏効症例に対しては3-4週間間隔で最大6-8コースが投与された。結果、%CR, %PRは各37%、27%で、3年生存割合は31%であった。CR持続期間中央値は20ヶ月で、40ヶ月の時点で無病生存の割合は10%しかなく、本レジメンでの高い奏効性により、より多くの症例を大量化学療法の適応とすることに意義があると思われた。主な毒性は骨髄抑制であり、好中球減少症(最低値中央値500/μl)、血小板減少症(最低値中央値70,000/μl)が認められた。この試験でもG-CSFなどの造血器growth factorは、当時上市されていなかったため、使用されなかった。そのため、好中球減少症は2-8日間持続し、30%(37例)の症例に好中球減少性発熱が認められ、入院の上、抗生剤投与を必要とし、5例が感染症で死亡した。高齢の1例が輸液負荷による循環器障害で死亡した。治療前値の2倍以上の血清クレアチニン上昇は、治療奏効のため2コース以上投与された症例を中心に22%(27例)に認められた。クレアチニン上昇は殆どの症例で一過性であったが、4%(5例)に永続的な上昇が認められ、これらの症例ではCDDP投与を中止した。嘔気・嘔吐、下痢などの消化器毒性は55%(67例)に認められたかが、軽微なものであった(Grade I-IIの嘔気・嘔吐は60例に、Grade IIIの嘔気・嘔吐は7例に認められた)。軽微〜中程度の疲労感、末梢神経症、低マグネシウム血症、低カリウム血症、貧血が奏効例を中心に認められた。CRに到達した1例が、化療終了後に病変部位の脳に照射を受け3年後に多巣性白質脳症と診断された。本試験では、122例中、治療関連死亡は6例(感染症5例、循環器障害1例)であり、G-CSFが使用可能な現在では、抗腫瘍化学療法を熟知した医師であれば安全性はさらに担保されるものと判断する。
4.
Philip T, Chauvin F, Armitage J, Bron D, Hagenbeek A, Biron P, Spitzer G, Velasquez W, Weisenburger DD, Fernandez-Ranada J, et al. Parma international protocol: pilot study of DHAP followed by involved-field radiotherapy and BEAC with autologous bone marrow transplantation. Blood. 1991 Apr 1;77(7):1587-92.
Parma studyに先だって1987年から1987年にかけて50例に実施されたpilot study(再発難治性中悪性度非ホジキンリンパ腫に対するDHAP療法後の自家造血幹細胞移植併用大量化学療法)でのDHAP療法での治療関連死亡はhemolytic uremic syndromeの1例であった。腎障害は7例(14%)に認められ、十分な利尿などの注意がCDDP使用に際して必要であるが、許容できる範囲内の毒性であると判断され、本試験であるランダム化比較試験(Parma study)が実施された。 |
| 他剤、他の組み合わせとの比較等について |
再発Aggressive NHLに対するsalvage regimen間でのランダム化試験の報告はなく、各報告のデータを示す。
EPOCH, CEPP-B, MINE, IMVP-16の%CR, %PR, median survival
 |
Gutierrez M, Chabner BA, Pearson D, et al. The role of a doxorubicin-containing regimen in relapsed and resistant lymphomas: an 8 year follow-up study of EPOCH. J Clin Oncol 2000;18:3633-42.
Blood 1997;10:4201-5.
Chao NJ, Rosenberg SA, Horning SJ. CEPP(B): an effective and well-tolerated regimen in poor-risk, aggressive non-Hodgkin’s lymphoma. Blood 1990;76:1293-8.
Cabanillas F, Hagemeister FB, Bodey GP, et al: IMVP-16: an effective regimen for patients with lymphoma who have relapsed after initial combination chemotherapy. Blood1982;60:693-7.
Cabanillas F, Hagemeister F, McLaughlin P, et al. Results of MIME salvage regimen for recurrent or refractory lym-phoma. J Clin Oncol 1987;5:407-12.
| 1. |
|
各治療法間の優劣はつけがたいが、Parma studyで使用されたことから、論文掲載でも使用頻度の高いレジメンはDHAP, ESHAPである。各レジメンでの奏効率は60-70%ほどであり、PR未満の症例に対しては、再度の救援化学療法が必要となることから、CDDPを含む救援化学療法が実施できない場合には、重要な選択可能な代表的治療法が使用できないこととなる。言い換えれば、病型や分子生物学的にヘテロな集団であるリンパ腫の救援化学療法としては、単一のレジメンのみで救援できるものではなく、2nd-lineのレジメンとして複数が必要であることも周知のことである。我が国ではCDDPが未承認であることから、EPOCHもしくは、愛知県がんセンター血液・細胞療法部で開発されたCHASE療法(Ogura M, Kagami Y, Taji H, et al. Phase I/II Study of New Salvage Therapy (CHASE) for Refractory or Relapsed Malignant Lymphomas. Int J Hematol.77;503-511, 2003)が救援化学療法として多く実施されているが、これらのレジメンで救援に失敗したときには、DHAP, ESHAPなどのCDDPを含むレジメンが必要となる。また、これらのレジメンの優劣をつけるためのランダム化比較試験を実施する際には、標準的治療群すなわち対照群はDHAPと見なされる。救援化学療法そのものを比較したランダム化比較試験の報告はなく、aggressive非ホジキンリンパ腫の初発治療におけるCHOP療法や、R-CHOP療法のようにランダム化比較試験によって確立した標準的治療法は救援化学療法には存在しない。しかし、再発時に救援化学療法のみで治療するか、救援化学療法に奏効した後に大量化学療法を追加するかのランダム化比較試験によって大量化学療法が標準的治療法であると確立した試験で採用された救援化学療法がDHAP療法であったため、世界的にDHAP療法は代表的な救援化学療法であるといえるし、そうしたコンセンサスが得られている(Gisselbrecht C, et al. Improving Second-Line Therapy in Aggressive Non-Hodgkin’s Lymphoma. Semin Oncol 31 (suppl 2):12-16. 2004)。 米国で開発されたICE療法とDHAP療法の各々にrituximabを併用した救援化学療法の大規模ランダム化比較試験が、再発性diffuse large B-cell lymphomaに対して欧州で開始されており、この試験(CORAL study)での標準的治療群はDHAP-RとされていることからもDHAP療法が、救援化学療法の標準的治療法として認識されていることを示している。 |
|